《2022年高中化學(xué) 第二章 化學(xué)物質(zhì)及其變化教案 新人教版必修1》由會員分享��,可在線閱讀����,更多相關(guān)《2022年高中化學(xué) 第二章 化學(xué)物質(zhì)及其變化教案 新人教版必修1(5頁珍藏版)》請?jiān)谘b配圖網(wǎng)上搜索。
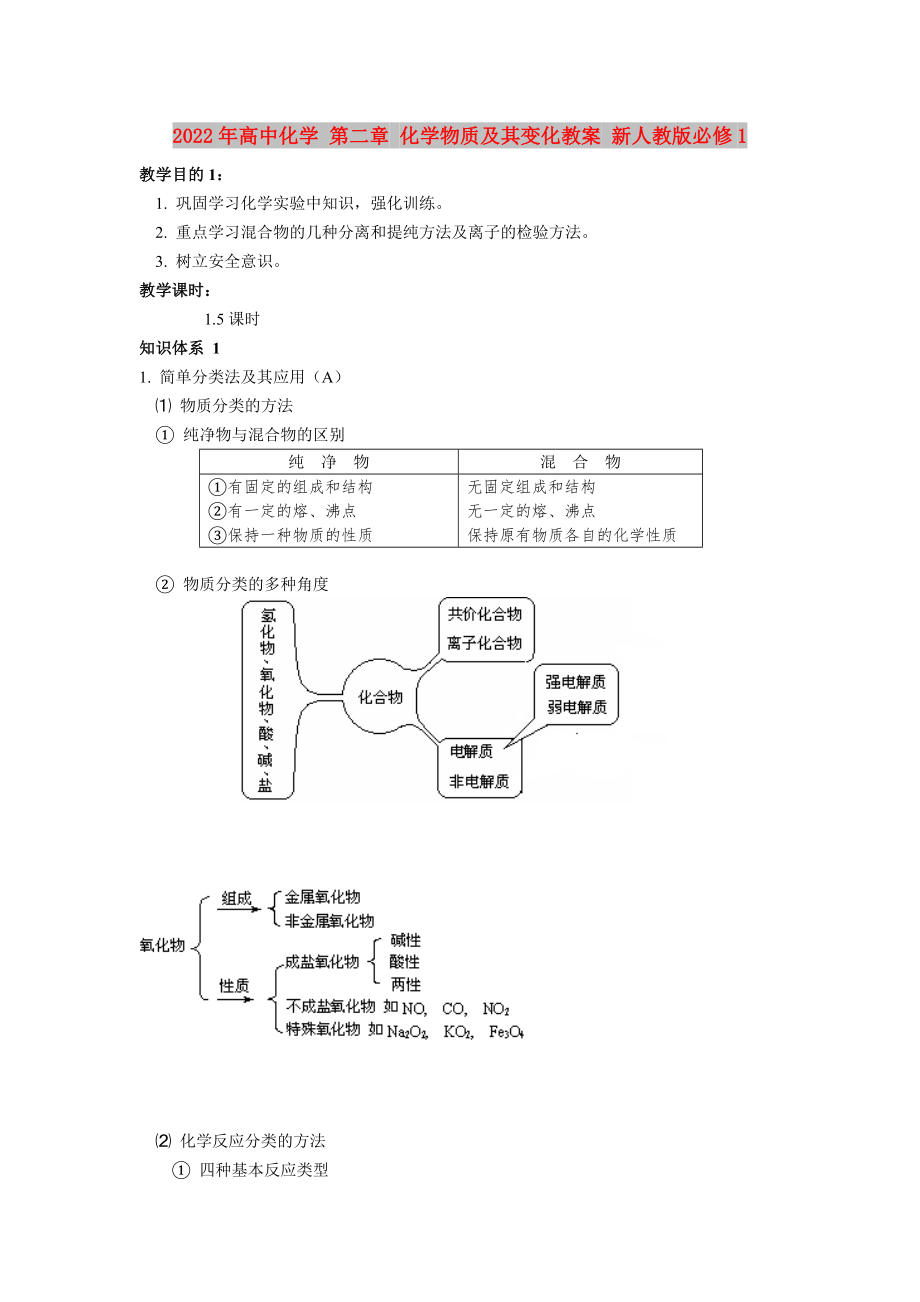
1�����、2022年高中化學(xué) 第二章 化學(xué)物質(zhì)及其變化教案 新人教版必修1教學(xué)目的1:1. 鞏固學(xué)習(xí)化學(xué)實(shí)驗(yàn)中知識�,強(qiáng)化訓(xùn)練。2. 重點(diǎn)學(xué)習(xí)混合物的幾種分離和提純方法及離子的檢驗(yàn)方法�。3. 樹立安全意識。教學(xué)課時(shí):1.5課時(shí)知識體系 11. 簡單分類法及其應(yīng)用(A) 物質(zhì)分類的方法 純凈物與混合物的區(qū)別純 凈 物混 合 物有固定的組成和結(jié)構(gòu)有一定的熔���、沸點(diǎn)保持一種物質(zhì)的性質(zhì)無固定組成和結(jié)構(gòu)無一定的熔�����、沸點(diǎn)保持原有物質(zhì)各自的化學(xué)性質(zhì) 物質(zhì)分類的多種角度 化學(xué)反應(yīng)分類的方法 四種基本反應(yīng)類型反應(yīng)類型舉 例表 示 式化合反應(yīng)C+O2 CO2A+B=AB分解反應(yīng)CaCO3 CaO+CO2AB=A+B置換反應(yīng)C+
2���、CuO Cu+COA+BC=AC+B復(fù)分解反應(yīng)AgNO3+NaCl=AgCl+NaNO3AB+CD=AD+CB 根據(jù)化合價(jià)是否變化 氧化還原反應(yīng)和非氧化還原反應(yīng) 四種基本反應(yīng)類型與氧化還原反應(yīng)(或非氧化還原反應(yīng))的關(guān)系氧化還原反應(yīng)非氧化還原反應(yīng)置換反應(yīng)分解反應(yīng)復(fù)分解反應(yīng)化合反應(yīng) 根據(jù)反應(yīng)中是否有離子參與 離子反應(yīng)和分子反應(yīng)2. 分散系及其分類(B)分散系 定義:一種(或幾種)物質(zhì)以粒子形式分散到另一種物質(zhì)里所形成的混合物。 組成:分散質(zhì)被分散成微粒的物質(zhì) 分散劑微粒分散在其中的物質(zhì) 分類:分散系溶液膠體懸(乳)濁液分散系粒子的直徑1nm1nm100nm100nm分散質(zhì)粒子的組成小分子或離子大分
3�、子或分子集合體許多分子的集合體外觀均一、透明大多均一���、透明不均一����、不透明能否透過濾紙能能一般不能能否透過半透膜能不能不能實(shí)例食鹽水�、糖水淀粉膠體、Fe(OH)3膠體泥水 膠體 膠體的本質(zhì)特征:分散質(zhì)微粒的直徑在1nm 100nm之間�����。膠體是以分散質(zhì)粒子大小為特征的,它只是物質(zhì)的一種存在形式���,如NaCl溶于水形成溶液�,如果分散在酒精中可形成膠體���??梢?���,同種分散質(zhì)在不同的分散劑中可以得到不同的分散系。 膠體的性質(zhì)現(xiàn)象定義解釋應(yīng)用丁達(dá)爾現(xiàn)象光束通過膠體時(shí)�����,形成光亮的通路的現(xiàn)象膠體分散質(zhì)的粒子比溶液中溶質(zhì)的微粒大���,使光波發(fā)生散射區(qū)別溶液和膠體布朗運(yùn)動在超顯微鏡下可觀察到膠體粒子在做不停的��、無秩序的運(yùn)動
4�����、�,叫做布朗運(yùn)動水分子從各個(gè)方向撞擊膠體粒子�,而每一瞬間膠體粒子在不同方向受的力是不相同的電泳現(xiàn)象在外加電場的作用下,膠體粒子在分散劑里向電極做定向移動的現(xiàn)象膠體粒子具有相對較大的表面積�,能吸附離子而帶電荷分離蛋白質(zhì)、氨基酸�����;血清電泳用于診斷疾?。浑娪倦婂兙?沉中和膠體粒子所帶的電荷�,使膠體粒子聚集長大,形成顆粒較大的沉淀從分散劑里析出的過程膠體粒子帶電�,加電解質(zhì)或帶相反電荷的膠體,中和了膠體粒子所帶的電荷�����,從而使分散質(zhì)聚集成較大的微粒���,在重力作用下沉淀析出制豆腐���、果凍等 膠體的分類類 型分散劑狀態(tài)實(shí) 例固溶膠固態(tài)有色玻璃、煙水晶液溶膠液態(tài)淀粉溶液、Fe(OH)3膠體氣溶膠氣態(tài)煙�����、云�、霧 膠體穩(wěn)
5、定存在的原因膠體粒子具有相對較大的表面積���,能吸附離子而帶電荷��,所以膠體粒子帶電����。同種膠體粒子帶同種電荷����,互相排斥而穩(wěn)定存在。一般說來�����,金屬的氫氧化物�、金屬氧化物的膠體粒子帶正電荷;非金屬氧化物�����、金屬硫化物、硅酸膠體的膠體粒子帶負(fù)電荷�����。 凈化膠體的方法滲析法將膠體放入半透膜袋里���,再將此袋放入水中,膠粒不能透過半透膜���,而分子����、離子可以透過半透膜�,從而使雜質(zhì)分子或離子進(jìn)入水中而除去。 膠體的應(yīng)用:土壤的保肥作用�、制豆腐的化學(xué)原理、江河入?�?谔幮纬扇侵?����、明礬凈水等。注意: 膠體中的分散質(zhì)可以是單個(gè)分子或離子或分子集合體 膠體聚沉后一般情況下都生成沉淀�,但有些膠體聚沉后,膠體粒子和分散劑凝聚在一起��,成
6����、為不流動的凍狀物,這類物質(zhì)叫凝膠���。 電泳現(xiàn)象是由于膠體能帶有電荷���,在外加電場作用下能向陽極或陰極移動。而有些膠體如淀粉溶液���,膠粒為中性分子�����,無電泳現(xiàn)象��。 基礎(chǔ)達(dá)標(biāo)1 1. 下列物質(zhì)屬于純凈物的是飲用天然水理化指標(biāo)礦物元素 測定結(jié)果鈣4.0 mg/L鎂0.5 mg/L鉀0.35 mg/L鈉0.8 mg/L偏硅酸1.8 mg/LpH (25) 7.1A.液氯 B.漂白粉 C.鹽酸 D.碘酒2右圖為農(nóng)夫山泉礦泉水瓶上的部分說明文字�,列出了該飲用天然水理化指標(biāo)���。這里的鈣���、鎂���、鉀、鈉是指A. 原子 B. 分子 C. 單質(zhì) D.元素3下列符號能同時(shí)表示一個(gè)原子�、一種元素和一種物質(zhì)的是A. O2 B. Zn
7、 C. N D. Ca2+ 4下列家庭小實(shí)驗(yàn)不能制得溶液的是 5科學(xué)家在2000年8月10日出版的英國自然雜志上報(bào)告說�,他們用DNA制造出一種臂長只有7nm的納米級鑷子,這種鑷子能鉗起分子或原子���,并對它們隨意組合下列分散系中分散質(zhì)的微粒直徑與納米粒子具有相同數(shù)量級的是 A溶液 B膠體 C. 懸濁液 D乳濁液6下列不存在丁達(dá)爾效應(yīng)的分散系是有塵埃的空氣�����、溴水��、蒸餾水��、沸水中加幾滴FeCl3濃溶液����、淀粉溶液 A. B. C. D.7自第十一屆奧運(yùn)會以來��,開幕式都要舉行隆重的火炬接力儀式���?���;鹁娴目扇嘉锸嵌⊥椋ɑ瘜W(xué)式為C4H10)����,它燃燒時(shí),火苗高且亮�,即使在白天,二百米以外也能清晰可見���。下列關(guān)于丁烷
8�����、的敘述不正確的是 A丁烷由碳�、氫兩種元素組成 B丁烷分子由碳原子和氫原子構(gòu)成C丁烷中碳�����、氫元素的質(zhì)量比是4:10 D丁烷由4個(gè)碳原子和10氫原子構(gòu)成8不能用有關(guān)膠體的觀點(diǎn)解釋的現(xiàn)象是 A. 在江河入海處易形成三角洲B. 0.01mol/LAgNO3溶液中滴入同濃度NaI溶液,看不到黃色沉淀C. 在NaF溶液中滴入AgNO3溶液看不到沉淀D. 同一鋼筆同時(shí)使用不同牌號的墨水易發(fā)生堵塞9下列各組混合物的分離和提純的方法正確的是 A. 用過濾的方法分離Fe(OH)3膠體和FeCl3溶液的混合物B. 用重結(jié)晶的方法分離NaCl和KNO3的混合物C. 用加熱的方法分離Na2CO3和NaHCO3的混合物D
9�����、. 用鹽析的方法分離淀粉和NaCl的混合液10能證明膠體微粒比溶液中電解質(zhì)微粒大的操作是A丁達(dá)爾現(xiàn)象 B布朗運(yùn)動 C滲析 D電泳現(xiàn)象11將某溶液逐滴加入Fe(OH)3溶膠內(nèi)���,開始時(shí)產(chǎn)生沉淀�����,繼續(xù)滴加時(shí)沉淀又溶解,則該溶液是A. 2mol/L的H2SO4溶液 B. 2mol/L的NaOH溶液C. 2mol/L的MgSO4溶液 D. 硅酸溶膠12下列物質(zhì)分離的方法中���,根據(jù)粒子的大小進(jìn)行分離的是A. 結(jié)晶 B. 過濾 C. 蒸餾 D. 滲析13下列化學(xué)反應(yīng)基本類型中一定是氧化還原反就的是A化合反應(yīng) B分解反應(yīng) C復(fù)分解反應(yīng) D置換反應(yīng)12345678910111213ADBBBCCCBCABDD課后有感 本節(jié)復(fù)習(xí)內(nèi)容屬于A了解要求的內(nèi)容�,考點(diǎn)要求不高��,主要是對概念的理解�。
 2022年高中化學(xué) 第二章 化學(xué)物質(zhì)及其變化教案 新人教版必修1
2022年高中化學(xué) 第二章 化學(xué)物質(zhì)及其變化教案 新人教版必修1