《(廣東專用)2015高考化學(xué)二輪復(fù)習(xí) 考前三個月 考前專項(xiàng)沖刺集訓(xùn) 第11題 電化學(xué)基礎(chǔ)》由會員分享�����,可在線閱讀�����,更多相關(guān)《(廣東專用)2015高考化學(xué)二輪復(fù)習(xí) 考前三個月 考前專項(xiàng)沖刺集訓(xùn) 第11題 電化學(xué)基礎(chǔ)(5頁珍藏版)》請?jiān)谘b配圖網(wǎng)上搜索���。
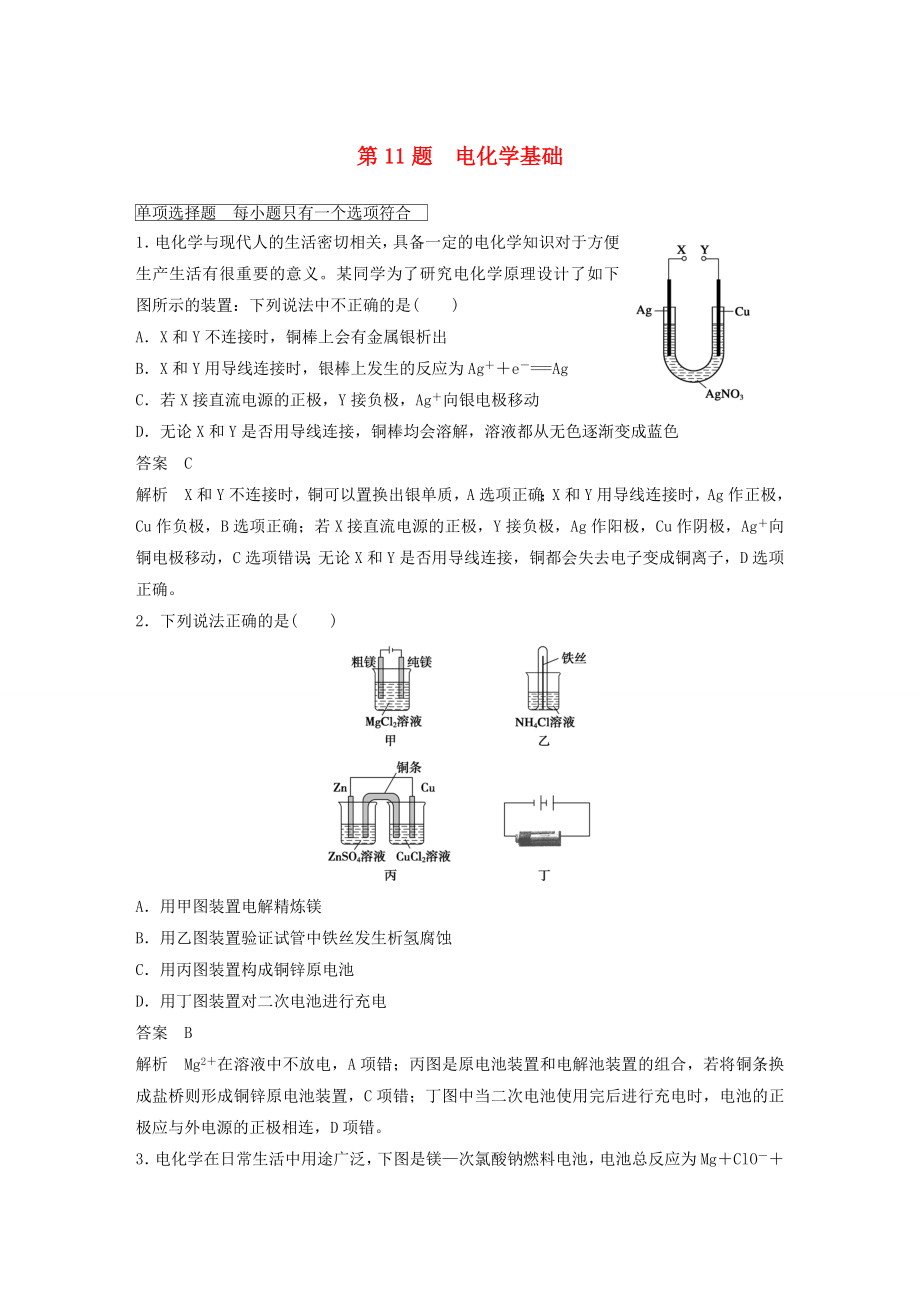
1���、第11題電化學(xué)基礎(chǔ)1電化學(xué)與現(xiàn)代人的生活密切相關(guān),具備一定的電化學(xué)知識對于方便生產(chǎn)生活有很重要的意義�����。某同學(xué)為了研究電化學(xué)原理設(shè)計(jì)了如下圖所示的裝置:下列說法中不正確的是()AX和Y不連接時����,銅棒上會有金屬銀析出BX和Y用導(dǎo)線連接時,銀棒上發(fā)生的反應(yīng)為Age=AgC若X接直流電源的正極��,Y接負(fù)極�����,Ag向銀電極移動D無論X和Y是否用導(dǎo)線連接,銅棒均會溶解���,溶液都從無色逐漸變成藍(lán)色答案C解析X和Y不連接時����,銅可以置換出銀單質(zhì)���,A選項(xiàng)正確;X和Y用導(dǎo)線連接時�,Ag作正極,Cu作負(fù)極�����,B選項(xiàng)正確���;若X接直流電源的正極���,Y接負(fù)極,Ag作陽極��,Cu作陰極,Ag向銅電極移動���,C選項(xiàng)錯誤�;無論X和Y是否用導(dǎo)線
2�����、連接,銅都會失去電子變成銅離子����,D選項(xiàng)正確��。2下列說法正確的是()A用甲圖裝置電解精煉鎂B用乙圖裝置驗(yàn)證試管中鐵絲發(fā)生析氫腐蝕C用丙圖裝置構(gòu)成銅鋅原電池D用丁圖裝置對二次電池進(jìn)行充電答案B解析Mg2在溶液中不放電����,A項(xiàng)錯;丙圖是原電池裝置和電解池裝置的組合���,若將銅條換成鹽橋則形成銅鋅原電池裝置�����,C項(xiàng)錯;丁圖中當(dāng)二次電池使用完后進(jìn)行充電時���,電池的正極應(yīng)與外電源的正極相連,D項(xiàng)錯��。3電化學(xué)在日常生活中用途廣泛���,下圖是鎂次氯酸鈉燃料電池�,電池總反應(yīng)為MgClOH2O=ClMg(OH)2,下列說法不正確的是()A鎂電極是該電池的負(fù)極B惰性電極上發(fā)生氧化反應(yīng)C正極反應(yīng)式為ClOH2O2e=Cl2OHD進(jìn)
3��、料口加入NaClO溶液����,出口為NaCl溶液答案B解析根據(jù)方程式知Mg是還原劑作負(fù)極�����,ClO在惰性電極上得電子發(fā)生還原反應(yīng)�����,生成Cl�����。4如圖所示���,甲池的總反應(yīng)式為N2H4O2=N22H2O下列關(guān)于該電池工作時說法正確的是()A甲池中負(fù)極反應(yīng)為N2H44e=N24HB甲池溶液pH不變,乙池溶液pH減小C甲池中消耗2.24 L O2����,此時乙池中理論上最多產(chǎn)生12.8 g固體D反應(yīng)一段時間后,向乙池中加一定量CuO固體�,能使CuSO4溶液恢復(fù)到原濃度答案D解析A項(xiàng)��,甲池中原電池反應(yīng)�����,對應(yīng)的電極反應(yīng)式是:正極O24e2H2O=4OH�,負(fù)極N2H44e4OH=N24H2O�����,錯誤����;B項(xiàng),甲池中因反應(yīng)生成了水
4��、會使溶液的pH值減小,乙池中因反應(yīng)生成了酸也會使溶液的pH值減小���,錯誤���;C項(xiàng),消耗氣體的體積沒有指明是否處于標(biāo)況�����,無法計(jì)算,錯誤��;D項(xiàng),乙池發(fā)生的是電解池反應(yīng)��,兩極析出的分別是Cu和O2���,因而加CuO后溶液能夠復(fù)原�,正確。5一種光化學(xué)電池的結(jié)構(gòu)如下圖�,當(dāng)光照在表面涂有氯化銀的銀片上時�,AgCl(s)Ag(s)Cl(AgCl)Cl(AgCl)表示生成的氯原子吸附在氯化銀表面���,接著Cl(AgCl)eCl(aq)���,若將光源移除���,電池會立即回復(fù)至初始狀態(tài)����。下列說法正確的是()A光照時�����,電流由Y流向XB光照時��,Pt電極發(fā)生的反應(yīng)為2Cl2e=Cl2C光照時��,Cl向Ag電極移動D光照時�����,電池總反應(yīng)為AgC
5�����、l(s)Cu(aq)Ag(s)Cu2(aq)Cl答案D解析由題意,光照時���,Cl原子在Ag極得到電子形成Cl����,Cl由Ag極向Pt極遷移,電子來源于Pt極上的Cu失去的電子����,經(jīng)導(dǎo)線流入Ag極,光照時電流的方向與電子的流向相反��,綜上分析�,A����、B、C錯誤,D項(xiàng)正確�。6用Na2SO3溶液吸收硫酸工業(yè)尾氣中的二氧化硫,將所得的混合液進(jìn)行電解循環(huán)再生��,這種新工藝叫再生循環(huán)脫硫法��。其中陰�、陽離子交換膜組合循環(huán)再生機(jī)理如圖所示�����,則下列有關(guān)說法中不正確的是()AX為直流電源的負(fù)極�����,Y為直流電源的正極B陽極區(qū)pH增大C圖中的baD該過程中的產(chǎn)品主要為H2SO4和H2答案B解析A項(xiàng)���,氫氣在Pt()極上生成���,說明Pt(
6���、)為陰極��,則X為負(fù)極,Y為正極�,正確;B項(xiàng)�����,陽極區(qū)的SO�����、HSO在陽極被氧化為SO����、H2SO4��,酸性增強(qiáng)��,pH減小�,錯誤����;C項(xiàng)�,由于陰�、陽離子交換膜的存在��,使加進(jìn)陽極區(qū)的硫酸的濃度小于陽極再生的硫酸的濃度,即ba�����,正確;D項(xiàng)����,陽極產(chǎn)品為硫酸��,陰極產(chǎn)品有氫氣和亞硫酸鈉�,正確���。7納米Cu2O是一種用途廣泛的光電材料����,可用如圖所示的兩種電化學(xué)裝置制備��,下列有關(guān)說法正確的是()A陽極的電極反應(yīng)式均為2Cu2e2OH=Cu2OH2OB工作過程中兩個裝置內(nèi)溶液的pH均減小C兩個裝置內(nèi)陰離子均移向銅電極D開始時陰極上均有氫氣生成答案C解析為得到純凈的Cu2O�,Cu2O應(yīng)在銅電極上生成,銅為陽極�,陰離子移向陽
7����、極���,C正確�����;右側(cè)裝置銅電極上的反應(yīng)式為2Cu2eH2O=Cu2O2H���,A錯誤;左側(cè)鐵電極上H放電����,總反應(yīng)式為2CuH2OCu2OH2,水被消耗導(dǎo)致NaOH濃度增大����,pH增大�����,B錯誤�����;右側(cè)裝置開始時是Cu2在陰極放電���,D錯誤����。8下圖是將SO2轉(zhuǎn)化為重要的化工原料H2SO4的原理示意圖�,下列說法不正確的是()A該裝置將化學(xué)能轉(zhuǎn)化為電能B電極b表面O2發(fā)生還原反應(yīng),其附近酸性增強(qiáng)C電極a表面的反應(yīng)是SO22H2O2e=SO4HD若得到的硫酸濃度仍為49%���,則理論上參加反應(yīng)的SO2與加入的H2O的質(zhì)量比為815答案B解析該裝置為原電池負(fù)極(a)2SO24e4H2O=8H2SO正極(b)O24e4H=2
8、H2O����,A項(xiàng)正確;B項(xiàng)�����,酸性應(yīng)減弱���,錯誤�����;C項(xiàng)正確;D項(xiàng)����,2SO2O22H2O=2H2SO4��,n(H2SO4)0.5 mol�����,正確�����。91807年化學(xué)家戴維用電解熔融氫氧化鈉的方法制得鈉:4NaOH(熔融)4NaO22H2O��;后來蓋呂薩克用鐵與熔融氫氧化鈉作用也制得鈉�����,反應(yīng)原理為3Fe4NaOH2H2Fe3O44Na�。下列有關(guān)說法中正確的是()A電解熔融氫氧化鈉制鈉,陽極上發(fā)生的電極反應(yīng)為2OH2e=H2O2B蓋呂薩克法制鈉原理是利用鐵的還原性比鈉強(qiáng)C若戴維法與蓋呂薩克法制得等量的鈉,則兩反應(yīng)中轉(zhuǎn)移的電子總數(shù)相同D.目前常用電解熔融氯化鈉的方法制鈉(如圖)���,電解槽中石墨為陽極��,鐵為陰極答案D解析由電解熔融NaOH的總反應(yīng)式知���,陽極上發(fā)生的反應(yīng)為4OHe=2H2OO2�����,A錯���;鐵的還原性比鈉弱,該反應(yīng)的發(fā)生是利用平衡移動原理(鈉的沸點(diǎn)低�����,形成氣體而脫離反應(yīng)體系)��,B錯�;由兩個反應(yīng)方程式知轉(zhuǎn)移的電子數(shù)不相等����,C錯。
 (廣東專用)2015高考化學(xué)二輪復(fù)習(xí) 考前三個月 考前專項(xiàng)沖刺集訓(xùn) 第11題 電化學(xué)基礎(chǔ)
(廣東專用)2015高考化學(xué)二輪復(fù)習(xí) 考前三個月 考前專項(xiàng)沖刺集訓(xùn) 第11題 電化學(xué)基礎(chǔ)