《人教版九年級(jí)化學(xué) 雙減分層作業(yè)設(shè)計(jì)樣例 案例 第三單元 課題2 原子的結(jié)構(gòu)》由會(huì)員分享����,可在線閱讀,更多相關(guān)《人教版九年級(jí)化學(xué) 雙減分層作業(yè)設(shè)計(jì)樣例 案例 第三單元 課題2 原子的結(jié)構(gòu)(4頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索��。
1��、
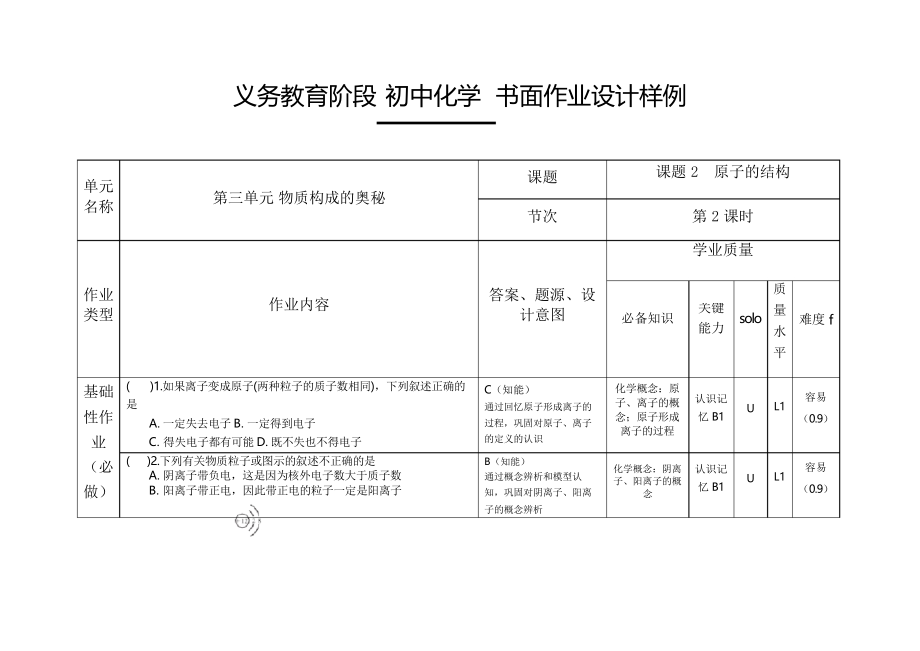
義務(wù)教育階段?初中化學(xué)?書面作業(yè)設(shè)計(jì)樣例
課題
單元
名稱
�
第三單元?物質(zhì)構(gòu)成的奧秘
�課題?2??原子的結(jié)構(gòu)
節(jié)次?????????????????第?2?課時(shí)
學(xué)業(yè)質(zhì)量
必備知識(shí)??? 關(guān)鍵
作業(yè)
類型
�
作業(yè)內(nèi)容
�答案、題源����、設(shè)
計(jì)意圖
�
能力??solo
�質(zhì)
量
水
�
難度?f
平
基礎(chǔ)
性作
業(yè)
(必
做)
�(???)1.如果離子變成原子(兩種粒子的質(zhì)子
2��、數(shù)相同)����,下列敘述正確的
是
A.?一定失去電子?B.?一定得到電子
C.?得失電子都有可能?D.?既不失也不得電子
(??)2.下列有關(guān)物質(zhì)粒子或圖示的敘述不正確的是
A.?陰離子帶負(fù)電,這是因?yàn)楹送怆娮訑?shù)大于質(zhì)子數(shù)
B.?陽(yáng)離子帶正電����,因此帶正電的粒子一定是陽(yáng)離子
�C(知能)
通過回憶原子形成離子的
過程,鞏固對(duì)原子�、離子
的定義的認(rèn)識(shí)
B(知能)
通過概念辨析和模型認(rèn)
知,鞏固對(duì)陰離子���、陽(yáng)離
�化學(xué)概念:原
子、離子的概
念;原子形成
離子的過程
化學(xué)概念:陰離
子�、陽(yáng)離子的概
念
�
認(rèn)識(shí)記
憶?B1???
3����、U
認(rèn)識(shí)記
憶?B1???U
�
L1???容易
(0.9)
L1???容易
(0.9)
子的概念辨析
C.?某粒子示意圖 ,表示的是一種陽(yáng)離子
D.?氯原子(?Cl?)得?1?個(gè)電子���,可形成氯離子(?Cl-?)
3.?在下列示意圖表示的粒子中,屬于原子的有________?(用序號(hào)填
空�����,下同)�,屬于陽(yáng)離子的有_________?�,屬于陰離子的有
________?,屬于相對(duì)穩(wěn)定的結(jié)構(gòu)的有_________�����。
�
(3)②⑤⑥����;?①④;
③�; ①
4�、③④(知能)
通過對(duì)微粒模型的理解和
分析,掌握原子�����、陰離
�微粒模型認(rèn)知:
原子����、離子的微
粒結(jié)構(gòu)模型認(rèn)知
�理解掌
握?B2???M
�L2???容易
(0.8)
4.用化學(xué)符號(hào)表示粒子:
�子�����、陽(yáng)離子、相對(duì)穩(wěn)定結(jié)
構(gòu)等的結(jié)構(gòu)特點(diǎn)
(1)Ca2+?(2)S2-
(1)鈣原子(Ca)失去?2?個(gè)電子變成的粒子是__________��。
(2)硫原子(S)得到?2?個(gè)電子變成的粒子是__________�。
(3)鈉原子(Na)失去?1?個(gè)電子變成的粒子是__________。
(4)氯原子(?Cl?)得到?
5����、1?個(gè)電子變成的粒子是__________。
�(3)Na+?(4)Cl-
(知能)
通過描述原子形成離子的
過程,書寫相應(yīng)的離子符
�
化學(xué)符號(hào)表達(dá)
式:離子符號(hào)的
表示方法
�
理解掌
握?B2???M
�
L2???中等
(0.7)
號(hào)����,強(qiáng)化對(duì)離子的形成的
理解,掌握離子符號(hào)的正
確書寫
( )5.下面粒子的結(jié)構(gòu)示意圖與書寫符號(hào)均正確的是
C(知能)
通過對(duì)微粒模型和符號(hào)相
對(duì)應(yīng)的判斷�,進(jìn)一步鞏固
對(duì)微粒模型的認(rèn)知以及微
�微粒模型認(rèn)知與
符號(hào)表達(dá)式:離
子結(jié)構(gòu)模型與離
子符號(hào)的書寫
�
理解
6����、掌
握?B2???M
�L2???中等
(0.7)
粒符號(hào)的正確書寫
A.?鈉離子 B.?氯離子 C.?鎂離子 D.?碳離子
( )6.分析鉀原子、鉀離子的結(jié)構(gòu)示意圖��,下列說法不正確的是
B(知能)
和離子結(jié)構(gòu)示意圖��,進(jìn)一
A.?兩者電子層數(shù)不同
B.?兩者質(zhì)子數(shù)不同
C.?兩者微粒種類不同
D.?兩者最外層電子數(shù)不同
( )7.右圖為某粒子的結(jié)構(gòu)示意圖�,有關(guān)該粒子的說法中錯(cuò)誤的是
�通過對(duì)比同種元素的原子????微粒模型認(rèn)知:
原子����、離子結(jié)構(gòu)
示意圖
步理解和掌握原子與離子
的區(qū)別
7�����、
D(知能)
�理解掌
握?B2
�M???L2???中等
(0.8)
A.?該粒子的原子核內(nèi)有?12?個(gè)質(zhì)子
B.?該粒子的核外有三個(gè)電子層
C.?該粒子在化學(xué)反應(yīng)中易失去?2?個(gè)電子
�通過對(duì)原子的結(jié)構(gòu)示意圖
的分析����,理解和掌握原子
的特點(diǎn)、分層排布以及最
�
微粒模型認(rèn)知:
原子的結(jié)構(gòu)特點(diǎn)
�
理解掌
握?B2???M
�
L2???容易
(0.8)
D.?該粒子在化學(xué)反應(yīng)中易形成陰離子
�外層電子數(shù)與化學(xué)性質(zhì)之
間的關(guān)系�。
拓展
性作
業(yè)
�(???)1.下列關(guān)于分子����、原子、離
8�����、子的說法不正確的是
A.?離子是帶電的原子或原子團(tuán),原子得失電子后形成離子
B.?構(gòu)成物質(zhì)的粒子除分子�����、原子之外��,還有離子
C.?在化學(xué)變化中分子可以再分�����,而原子不能再分
D.?分子是保持物質(zhì)性質(zhì)的最小粒子
�
D(知能)
通過描述分子���、原子��、離
子的概念的聯(lián)系及區(qū)別�,
鞏固原子、分子���、離子的
�
微粒的分類:分
子�����、原子與離子
的聯(lián)系與區(qū)別
�
認(rèn)知記
憶?B1???U
�
L1???容易
(0.8)
認(rèn)知
(選
做)
�2..金屬鈉與氯氣在一定條件下可以發(fā)生化學(xué)反應(yīng)�。該反應(yīng)的文字表
9���、達(dá)式為:鈉+氯氣?????氯化鈉�。根據(jù)所給信息�,請(qǐng)回答下列問題:
理解掌
握?B2
�M???L2???中等
(0.7)
失去�����; 正���; 得到���;
負(fù); Na+?和?Cl-
(知能)
通過對(duì)課本示例的示意圖
改編�,用模型結(jié)構(gòu)示意圖
來(lái)展示原子形成離子,
陰��、陽(yáng)離子形成離子化合
物的過程�,進(jìn)一步理解與
掌握原子形成離子的過
程,鞏固離子化合物是有
�
微粒模型認(rèn)知與
物質(zhì)的構(gòu)成:陽(yáng)
離子與陰離子的
形成及特點(diǎn)�,離
子化合物的微粒
構(gòu)成
當(dāng)鈉與氯氣反應(yīng)時(shí),每個(gè)鈉原子________?(填“得到”或“失去”)電
10�、
子成為鈉離子�����,帶____(填“正”或“負(fù)”)電��,每個(gè)氯原子_________
(填“得到”或“失去”)電子成為氯離子���,帶______(填“正”或
“負(fù)”)電。帶相反電荷的鈉離子和氯離子相互作用就形成了氯化
鈉�����,可見����,構(gòu)成氯化鈉的微粒是_________?(填離子符號(hào))。
�陰陽(yáng)離子構(gòu)成的認(rèn)知����。
( )3.某微粒的結(jié)構(gòu)示意圖為 ,若?x?等于?11����,則該微粒表示
A.?原子 B.?分子 C.?陽(yáng)離子 D.?陰離子
�C(知能)
通過對(duì)未知微粒結(jié)構(gòu)示意
圖的分析���,掌握不同類型
�模型認(rèn)知:原
子��、離子的結(jié)構(gòu)
特點(diǎn)
�模仿應(yīng)
用?B3
�R???L3???中等
(0.6)
微粒的結(jié)構(gòu)特點(diǎn)
 人教版九年級(jí)化學(xué) 雙減分層作業(yè)設(shè)計(jì)樣例 案例 第三單元 課題2 原子的結(jié)構(gòu)
人教版九年級(jí)化學(xué) 雙減分層作業(yè)設(shè)計(jì)樣例 案例 第三單元 課題2 原子的結(jié)構(gòu)