《新編高二化學(xué)蘇教版選修四作業(yè):專題3 第2單元第2課時(shí) 酸堿中和滴定》由會(huì)員分享����,可在線閱讀���,更多相關(guān)《新編高二化學(xué)蘇教版選修四作業(yè):專題3 第2單元第2課時(shí) 酸堿中和滴定(3頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索�����。
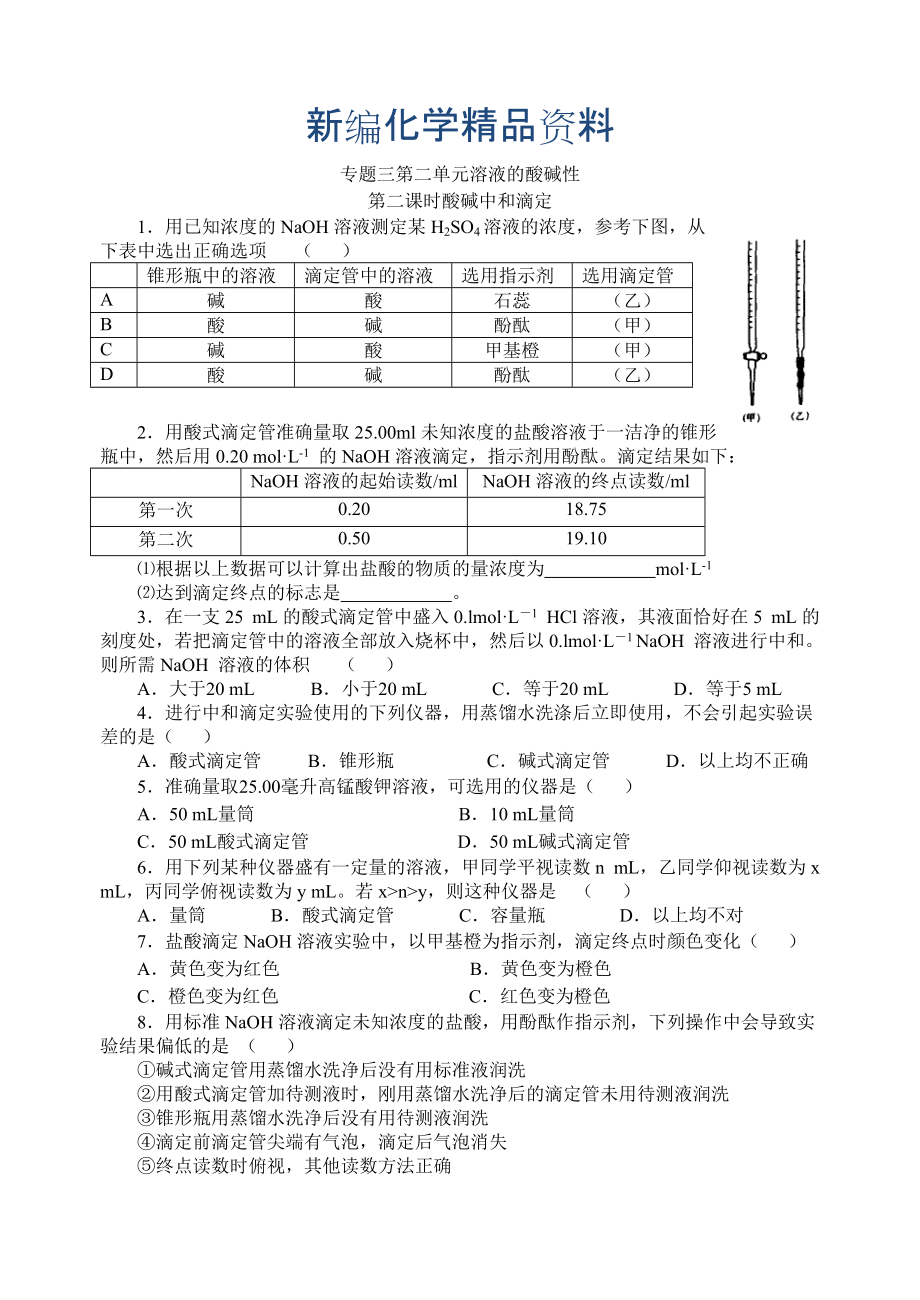
1�����、新編化學(xué)精品資料專題三第二單元溶液的酸堿性第二課時(shí)酸堿中和滴定1用已知濃度的NaOH溶液測(cè)定某H2SO4溶液的濃度���,參考下圖���,從下表中選出正確選項(xiàng) ( )錐形瓶中的溶液滴定管中的溶液選用指示劑選用滴定管A堿酸石蕊(乙)B酸堿酚酞(甲)C堿酸甲基橙(甲)D酸堿酚酞(乙)2用酸式滴定管準(zhǔn)確量取25.00ml未知濃度的鹽酸溶液于一潔凈的錐形瓶中,然后用0.20 molL-1 的NaOH溶液滴定��,指示劑用酚酞����。滴定結(jié)果如下:NaOH溶液的起始讀數(shù)/mlNaOH溶液的終點(diǎn)讀數(shù)/ml第一次0.2018.75第二次0.5019.10根據(jù)以上數(shù)據(jù)可以計(jì)算出鹽酸的物質(zhì)的量濃度為 molL-1達(dá)到滴定終點(diǎn)的標(biāo)志是
2、 ��。3在一支25 mL的酸式滴定管中盛入0.lmolL1 HCl溶液�,其液面恰好在5 mL的刻度處,若把滴定管中的溶液全部放入燒杯中�,然后以0.lmolL1 NaOH 溶液進(jìn)行中和�。則所需NaOH 溶液的體積 ( ) A大于20 mL B小于20 mL C等于20 mL D等于5 mL4進(jìn)行中和滴定實(shí)驗(yàn)使用的下列儀器,用蒸餾水洗滌后立即使用����,不會(huì)引起實(shí)驗(yàn)誤差的是( ) A酸式滴定管 B錐形瓶 C堿式滴定管 D以上均不正確5準(zhǔn)確量取25.00毫升高錳酸鉀溶液,可選用的儀器是( )A50 mL量筒 B10 mL量筒 C50 mL酸式滴定管 D50 mL堿式滴定管6用下列某種儀器盛有一定量的溶液����,甲
3���、同學(xué)平視讀數(shù)n mL,乙同學(xué)仰視讀數(shù)為x mL���,丙同學(xué)俯視讀數(shù)為y mL���。若xny,則這種儀器是 ( ) A量筒 B酸式滴定管 C容量瓶 D以上均不對(duì)7鹽酸滴定NaOH溶液實(shí)驗(yàn)中�,以甲基橙為指示劑,滴定終點(diǎn)時(shí)顏色變化( )A黃色變?yōu)榧t色 B黃色變?yōu)槌壬獵橙色變?yōu)榧t色 C紅色變?yōu)槌壬?用標(biāo)準(zhǔn)NaOH溶液滴定未知濃度的鹽酸���,用酚酞作指示劑����,下列操作中會(huì)導(dǎo)致實(shí)驗(yàn)結(jié)果偏低的是 ( ) 堿式滴定管用蒸餾水洗凈后沒有用標(biāo)準(zhǔn)液潤(rùn)洗 用酸式滴定管加待測(cè)液時(shí)����,剛用蒸餾水洗凈后的滴定管未用待測(cè)液潤(rùn)洗錐形瓶用蒸餾水洗凈后沒有用待測(cè)液潤(rùn)洗 滴定前滴定管尖端有氣泡,滴定后氣泡消失 終點(diǎn)讀數(shù)時(shí)俯視���,其他讀數(shù)方法正確 A
4�、B C D9用0.1 molL-1 NaOH溶液滴定0.l molL-1鹽酸,如達(dá)到滴定的終點(diǎn)時(shí)不慎多加了1滴NaOH溶液(1滴溶液的體積約為0.05mL)�。繼續(xù)加水至50mL,所得溶液的pH是( ) A4B7.2 C10 D11.310實(shí)驗(yàn)室常利用甲醛法測(cè)定(NH4)2SO4樣品中氮的質(zhì)量分?jǐn)?shù)���,其反應(yīng)原理為:4NH4 6HCHO =3H6H2O(CH2)6N4H 滴定時(shí)����,1 mol (CH2)6N4H與 l mol H相當(dāng)���,然后用NaOH標(biāo)準(zhǔn)溶液滴定反應(yīng)生成的酸�����。某興趣小組用甲醛法進(jìn)行了如下實(shí)驗(yàn):步驟I 稱取樣品1.500 g�����。步驟II 將樣品溶解后�����,完全轉(zhuǎn)移到250 mL容量瓶中,定容��,充
5、分搖勻����。步驟III 移取25.00 mL樣品溶液于250 mL錐形瓶中,加入10 mL 20的中性甲醛溶液����,搖勻、靜置5 min后���,加入12滴酚酞試液����,用NaOH標(biāo)準(zhǔn)溶液滴定至終點(diǎn)���。按上述操作方法再重復(fù)2次�。根據(jù)步驟III 填空:堿式滴定管用蒸餾水洗滌后�����,直接加入NaOH標(biāo)準(zhǔn)溶液進(jìn)行滴定���,則測(cè)得樣品中氮的質(zhì)量分?jǐn)?shù) (填“偏高”���、“偏低”或“無(wú)影響”)�����。錐形瓶用蒸餾水洗滌后�,水未倒盡����,則滴定時(shí)用去NaOH標(biāo)準(zhǔn)溶液的體積 (填“偏大”、“偏小”或“無(wú)影響”)滴定時(shí)邊滴邊搖動(dòng)錐形瓶��,眼睛應(yīng)觀察 (A)滴定管內(nèi)液面的變化 (B)錐形瓶?jī)?nèi)溶液顏色的變化滴定達(dá)到終點(diǎn)時(shí)��,酚酞指示劑由 色變成 色���。滴定結(jié)果如
6����、下表所示:滴定次數(shù)待測(cè)溶液的體積/mL標(biāo)準(zhǔn)溶液的體積/mL滴定前刻度滴定后刻度125. 001.0221.03225.002.0021.99325.000.2020.20若NaOH標(biāo)準(zhǔn)溶液的濃度為0.1010 molL1�����,則該樣品中氮的質(zhì)量分?jǐn)?shù)為 �����。11用中和滴定的方法測(cè)定NaOH和Na2CO3的混合液中NaOH含量時(shí)���,可先在混合液中加過(guò)量BaCl2溶液�,使Na2CO3完全變成BaCO3沉淀�����,然后用標(biāo)準(zhǔn)鹽酸滴定(用酚酞作指示劑)向混有BaCO3沉淀的NaOH溶液中滴入鹽酸�����,_(填“會(huì)”或“不會(huì)”)使BaCO3溶解而影響測(cè)定NaOH的含量�����,理由是_��。確定終點(diǎn)時(shí)溶液的顏色由_變?yōu)開���。滴定時(shí)�����,若滴定
7���、過(guò)程中滴定液一直下降到活塞處才到達(dá)滴定終點(diǎn)����,_(填“能”或“不能”)由此得出準(zhǔn)確的測(cè)定結(jié)果�。_(填“能”或“不能”)改用甲基橙作指示劑。若使用甲基橙作指示劑�����,則測(cè)定結(jié)果_(填“偏高”��、“偏低”或“正確”)�����。參考答案1.CD 2.0.1486mol/L最后一滴NaOH溶液滴入時(shí)�����,溶液由無(wú)色變?yōu)闇\紅色�����,且半分鐘內(nèi)不退色。3.A 4.B 5.C 6.B 7.B 8.D 9.C 10. 偏高 無(wú)影響 B 無(wú) 粉紅或淺紅 18.8511.不會(huì)����,當(dāng)酚酞變色時(shí)的pH值條件下����,HCl是與NaOH發(fā)生反應(yīng),不會(huì)與BaCO3作用��。淺紅色 無(wú)色 不能����。因滴定管下方刻度線距活塞處有一定空間,不能測(cè)出其所用的滴定液體積不能 偏高
 新編高二化學(xué)蘇教版選修四作業(yè):專題3 第2單元第2課時(shí) 酸堿中和滴定
新編高二化學(xué)蘇教版選修四作業(yè):專題3 第2單元第2課時(shí) 酸堿中和滴定